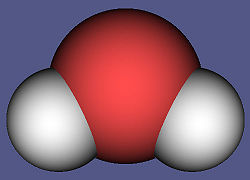
Вода
| Вода (Н2O) | |
|---|---|
| Схематичное изображение молекулы воды | |
| Наименование | Вода (Н2O) |
| Формула | Н2O |
| Плотность | 998,2 кг/м³ (при 20 °C) |
| Tплавления | 0 °C |
| Tкипения | 100 °C |
| Удельный вес | 9790 H/м³ |
| Молекулярный вес | 18,01528 а.е.м. |
| Теплопроводность | 0,56 Вт/м·°C (при 0 °C) |
| Удельная теплоемкость | 4200 Дж/(кг·°C) |
| Динамическая вязкость | 0,00101 Па·с (при 20 °C) |
| Кинематическая вязкость | 0,01012 см²/с (при 20 °C) |
Вода — прозрачная бесцветная жидкость, не имеет цвета и запаха. Химическая формула: Н2O. В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром.
Вода — очень распространённое вещество на Земле, 71 % поверхности которой покрыто водой, составляющей океаны, моря, озера, реки и т. п.
Также вода в газообразном состоянии находится в атмосфере планеты в виде облаков, туманов и т. п. При конденсации выводится из атмосферы в виде атмосферных осадков (дождь, снег, град, роса и т. д.). В совокупности жидкая водная оболочка Земли называется гидросферой, а твёрдая криосферой. Является активным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы и т. д).
Особенности водыПравить
Интересной особенностью воды является то, что при нагревании от 0 до 4 (3,98 — точно) °C вода сжимается. Благодаря этому могут жить рыбы: когда температура падает ниже 4 °C, более холодная вода, как менее плотная, остаётся на поверхности и замерзает, а подо льдом сохраняется положительная температура.
У воды есть и другие особенности: высокая температура и удельная теплота плавления и кипения (по сравнению с соединениями водорода с похожим молекулярным весом); высокая теплоёмкость и низкая вязкость жидкой воды; вода, в отличие от других веществ, при замерзании расширяется. Вода практически несжимаема. Все эти особенности обусловлены водородными связями. Поскольку в молекуле воды 2 атома водорода отдают по одному электрону атому кислорода, атом кислорода получает отрицательный заряд, а атомы водорода — положительный. Благодаря этому, каждый атом кислорода притягивается к атомам водорода других молекул и наоборот. Каждая молекула воды может участвовать максимум в четырёх водородных связях: 2 атома водорода — каждый в одной, а атом кислорода — в двух. При таянии льда часть связей рвётся, что позволяет уложить молекулы воды плотнее; при нагревании воды связи продолжают рваться, и плотность её растёт, но при температуре выше 4 °С этот эффект слабее, чем обычное тепловое расширение; при испарении рвутся все оставшиеся связи. Разрыв связей требует много энергии, отсюда высокая температура и удельная теплота плавления и кипения и высокая теплоёмкость. Вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями.
По сходным причинам вода является хорошим растворителем. Каждая молекула растворяемого вещества окружается молекулами воды, причём положительно заряженные участки молекулы растворяемого вещества притягиваются к атомам водорода, а отрицательно заряженные — к атомам кислорода. Поскольку молекула воды мала по размерам, много молекул воды могут окружить каждую молекулу растворимого вещества.
Это свойство воды используется живыми существами. В живой клетке и в межклеточном пространстве вступают во взаимодействие растворы различных веществ в воде.(не подтверждено) Поэтому вода необходима для жизни всех без исключения одноклеточных и многоклеточных живых существ на Земле. Вода имеет показатель преломления n=1,33 в оптическом диапазоне. Однако она сильно поглощает инфракрасное излучение, и поэтому водяной пар является основным естественным парниковым газом, отвечающим более чем за 60 % парникового эффекта. Благодаря большому дипольному моменту молекул, вода также поглощает микроволновое излучение, на чем основан принцип действия микроволновой печи.[1].
Чистая вода была бы хорошим изолятором. Но благодаря тому, что вода — растворитель, в ней практически всегда растворены те или иные соли, что обуславливает наличие в воде различных положительных и отрицательных ионов, благодаря чему она проводит электрический ток. При температуре 647 K (374 °C или 705 °F) и давлении 22.064 MПa (3200 PSIA или 218 атм) вода проходит критическую точку и не может оставаться в жидком состоянии.
Приватизация водыПравить
Вода не должна быть человеческим правом, согласно мнению продуктового гиганта «Nestle». Мы поговорили с председателем компании «Nestle» и у него нет места филантропическим идеям. Питер Брабэк-Летмеф:
«Согласно всемирной декларации, вода — всеобщее право. Это означает, как человек вы имеете право на воду. Лично я считаю, что вода должна что-то стоить, тогда населением, которое не будет иметь доступ к воде, можно будет управлять.»
Давайте поговорим с Энтони Гучиади из naturalsociety.com. Что вы думаете по этому поводу? Энтони Гучиади:
«Если вода должна принадлежать этим большим корпорациям, почему бы тогда не приватизировать воду? Почему всё в нашей жизни не превратить в источник прибыли больших корпораций?»
Поступают первые инвестиции в фонд воды. Шаг на пути, чтобы превратить в источник прибыли один из главных элементов жизни. Мы знаем, что происходит, когда главные источники жизни превращают в источники прибыли. Такое уже случалось.[2]
ПримечанияПравить
См. такжеПравить
Ошибка Lua в Модуль:Родственные_проекты на строке 23: attempt to index field 'wikibase' (a nil value).
СсылкиПравить
ЛитератураПравить
- Вода знакомая и загадочная Леонид КУЛЬСКИЙ, Воля ДАЛЬ, Людмила ЛЕНЧИНА