Мышечное сокращение
Мы́шечное сокраще́ние (МС) — укорочение мышцы, в результате которого она производит механическую работу. МС обеспечивает способность животных и человека к произвольным движениям. Наиболее важная составная часть мышечной ткани — белки (16,5-20,9%), в т. ч. контрактильные (контрактильный (contractilis; лат. contraho, contractum стягивать, сокращать), обусловливающие способность мышцы к сокращению. Или реакция мышечных клеток на воздействие нейромедиатора, реже гормона, проявляющаяся в уменьшении длины клетки. Это жизненно важная функция организма, связанная с оборонительными, дыхательными, пищевыми, половыми, выделительными и другими физиологическими процессами.
Все виды произвольных движений — ходьба, мимика, движения глазных яблок, глотание, дыхание и т. п. осуществляются за счёт скелетных мышц. Непроизвольные движения (кроме сокращения сердца) — перистальтика желудка и кишечника, изменение тонуса кровеносных сосудов, поддержание тонуса мочевого пузыря — обусловлены сокращением гладкой мускулатуры. Работа сердца обеспечивается сокращением сердечной мускулатуры.
ВведениеПравить
В 1-й половине XX века В. А. Энгельгардт и М. Н. Любимова (1939) установили, что основной контрактильный белок мышц — миозин — обладает аденозинтрифосфатазной активностью, а А. Сент-Дьёрдьи и Ф. Б. Штрауб показали (1942—43), что входящий в состав миофибрилл белок состоит в основном из 2 компонентов — миозина и актина. Взаимодействие этих фибриллярных белков и лежит в основе феномена сокращения самых различных контрактильных органелл и органов движения.
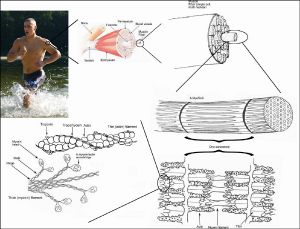
В скелетных мышцах за сокращение отвечают миофибриллы (примерно две трети сухого веса мышц). Миофибриллы — структуры толщиной 1 — 2 мкм, состоящие из саркомеров — структур длиной около 2,5 мкм, состоящих из актиновых и миозиновых (тонких и толстых) филаментов и Z-дисков, соединённых с актиновыми филаментами. Сокращение происходит при увеличении концентрации в цитоплазме ионов Ca2+ в результате скольжения миозиновых филаментов относительно актиновых. Источником энергии сокращения служит АТФ. КПД мышечной клетки около 50 %, мышцы в целом не более 20%. Максимальная сила мышц не достигается в реальных условиях; не все клетки мышцы используются одновременно и сокращаются с максимальной силой, иначе при сокращении многих скелетных мышц будут повреждены сухожилия или кости (что иногда и наблюдается при сильных судорогах). КПД мышцы также зависит от внешних условий; например, на холоде он значительно снижается, так как для организма важнее сохранить температуру тела.[1]
Скольжение миозина относительно актинаПравить
Головки миозина расщепляют АТФ и за счет высвобождающейся энергии меняют конформацию, скользя по актиновым филаментам. Цикл можно разделить на 4 стадии:
- Свободная головка миозина связывается с АТФ и гидролизует его до АДФ (Аденозиндифосфат (АДФ) — нуклеотид, состоящий из аденина, рибозы и двух остатков фосфорной кислоты) и фосфата и остаётся связанной с ними. (Обратимый процесс — энергия, выделившаяся в результате гидролиза, запасается в изменённой конформации миозина).
- Головки слабо связываются со следующей субъединицей актина, фосфат отделяется, и это приводит к прочному связыванию головки миозина с актиновым филаментом. Эта реакция уже необратима.
- Головка претерпевает конформационное изменение, производящее подтягивание толстого филамента к Z-диску (или, что эквивалентно, свободных концов тонких филаментов друг к другу).
- Отделяется АДФ, за счёт этого головка отделяется от актинового филамента. Присоединяется новая молекула АТФ.
Далее цикл повторяется до уменьшения концентрации ионов Ca2+ или исчерпании запаса АТФ (в результате смерти клетки). Скорость скольжения миозина по актину ≈15 мкм/сек. В миозиновом филаменте много (около 500) молекул миозина и, следовательно, при сокращении цикл повторяется сотнями головок сразу, что и приводит к быстрому и сильному сокращению. Следует заметить, что миозиин ведёт себя как фермент — актин-зависимая АТФаза. В связи с тем, что каждое повторение цикла связано с гидролизом АТФ, откуда с положительным изменением свободной энергии, процесс однонаправленный. Миозин движется по актину только в сторону плюс-конца.
Источник энергии для сокращенияПравить
Взаимодействие этих фибриллярных белков атина и меозина лежит в основе феномена сокращения самых различных контрактильных органелл и органов движения (см. Мышцы). Периодические изменение физического состояния мышечных белков, обусловливающее возможность попеременного сокращения и расслабления мышц и выполнения ими механической работы, очевидно, связано с определёнными дающими энергию биохимическими процессами. Энгельгардтом и Любимовой (1939—42) было обнаружено, что особым образом приготовленные из миозина нити при взаимодействии с раствором АТФ резко изменяют свои механические свойства (эластичность и растяжимость). Одновременно происходит расщепление АТФ с образованием АДФ и неорганического фосфата. Это открытие заложило фундамент для нового направления в биохимии — механохимии М. с. В дальнейшем Сент-Дьёрдьи и Штрауб показали, что истинным сократительным белком является не миозин, а его комплекс с актином — актомиозин. Сокращению при взаимодействии с АТФ подвергаются как вымоченные в воде или 50%-ном глицерине мышечные волокна, так и нити, приготовленные из актомиозиновых гелей (синерезис геля). Эти опыты подтверждают, что энергия, необходимая для сокращения мышц, освобождается в результате взаимодействия актомиозина с АТФ с расщеплением последнего на АДФ и H3PO4. При этом освобождается большое количество энергии (8—10 ккал, или 33,5—41,9 кдж, на 1 моль АТФ). Однако истинный механизм этой реакции остаётся всё ещё неясным.
Механизм регуляцииПравить
В основном в регуляции мышечной активности участвуют нейроны, но есть случаи, когда сокращением гладкой мускулатуры управляют и гормоны (например, адреналин и окситоцин). Сигнал о сокращении можно разделить на несколько этапов:
От клеточной мембраны до саркоплазматического ретикулумаПравить
Воздействие медиатора, выделившегося из мотонейрона, вызывает потенциал действия на клеточной мембране мышечной клетки, который передаётся далее с помощью специальных впячиваний мембраны, называемых Т-трубочками, которые отходят от мембраны внутрь клетки. От Т-трубочек сигнал передаётся саркоплазматическому ретикулуму — особому компартменту из уплощенных мембранных пузырьков (эндоплазматической сети мышечной клетки), окружающих каждую миофибриллу. Этот сигнал вызывает открытие Ca2+ — каналов в мембране ретикулума. Обратно ионы Ca2+ попадают в ретикулум с помощью мембранных кальциевых насосов — Ca2+-АТФазы.
От выделения ионов Ca2+ до сокращения миофибриллПравить
Для контроля сокращения мышц к актиновому филаменту прикрепляется белок тропомиозин и комплекс из трёх белков — тропонин (субъединицы комплекса этих трёх белков называются тропонинами T,I и C). Тропонин C — близкий гомолог другого белка, кальмодулина. Через каждые семь субъединиц актина расположен только один тропониновый комплекс. Связь актина с тропонином I перемещает тропомиозин в положение, которое мешающет связи миозина с актином. Тропонин C связывается с четырьмя ионами Ca2+ и ослабляет действие тропонина I на актин, а тропомиозин занимает положение, не препятствующее связи актина с миозином. Источником энергии для сокращения мышечных волокон служит АТФ. При связывании тропонина с ионами кальция активируются каталитические центры для расщепления АТФ на головках миозина. За счет ферментативной активности головок миозина гидролизуется АТФ, расположенный на головке миозина, что обеспечивает энергией изменение конформации головок и скольжение нитей. Освобождающиеся при гидролизе АТФ молекула АДФ и неорганический фосфат используются для последующего ресинтеза (повторное возобновляемое воспроизводимое действие) АТФ. К миозиновой головке присоединяется новая молекула АТФ. При этом происходит разъединение поперечного мостика с нитью актина. Повторное прикрепление и отсоединение мостиков продолжается до тех пор, пока концентрация кальция внутри миофибрилл не снизится до подпороговой величины. Когда мышечные волокна начинают расслабляться.[2][3]
Основные белки миофибриллПравить
| Белок | Доля белка % | Его мол. масса, kDa | Его функция |
|---|---|---|---|
| Миозин | Главный компонент толстых филаментов. Образует связи с актином. Движется по актину за счёт гидролиза АТФ. | ||
| Актин | Главный компонент тонких филаментов. Во время сокращения мышцы по нему движется миозин. | ||
| Титин | Большой гибкий белок, образующий цепь для связывания миозина с Z-диском. | ||
| Тропонин | Комплекс из трёх белков, регулирующий сокращение при связывании с ионами Ca2+. | ||
| Тропомиозин | Связанный с актиновыми филаментами стержневидный белок, блокирующий движение миозина. | ||
| Небулин | Длинный нерастяжимый белок, связанный с Z-диском и идущий параллельно актиновым филаментам. |
ПримечанияПравить
- ↑ Коэффициент полезного действия работы в процессе адаптации человека к мышечной деятельности Научная библиотека диссертаций и авторефератов disserCat http://www.dissercat.com/content/koeffitsient-poleznogo-deistviya-raboty-v-protsesse-adaptatsii-cheloveka-k-myshechnoi-deyate#ixzz2xrMGjDYa
- ↑ http://bse.slovaronline.com/%D0%9C/%D0%9C%D0%AB/45563-MYSHECHNOE_SOKRASCHENIE
- ↑ https://en.wikipedia.org/wiki/Muscle_contraction
ЛитератураПравить
- Б. Альбертс, Д. Брей, Дж. Льюис, М. Рефф, К. Робертс, Дж. Уотсон, Молекулярная биология клетки — В 3-х т. — Пер. с англ. — Т.2. — М.: Мир, 1994. — 540 с.
- М. Б. Беркинблит, С. М. Глаголев, В. А. Фуралев, Общая биология — В 2-х ч. — Ч.1. — М.:МИРОС, 1999. — 224 с.: ил.